Descripción General del CMV
Descripción General del CMV
Ahora, vamos a repasar algunos aspectos importantes que deben tenerse en cuenta al atender a los pacientes con CMV.
- La infección primaria por CMV es la detección inicial de infección por CMV en una persona que no ha estado expuesta anteriormente al virus.1,2
- Después de la infección primaria, el CMV puede mantenerse latente. Las personas inmunodeprimidas, como los receptores de TCMH alogénicos, después del trasplante, corren el riesgo de reactivación, también conocida como infección por CMV, y de progresión subsecuente a enfermedad por el CMV y otras complicaciones relacionadas.1,3
- Se considera que la infección por CMV progresó a reactivación cuando la carga viral se vuelve detectable en la sangre. Las cargas virales del CMV se pueden determinar por diversos métodos, que incluye antigenemia, ribonuclemia o desoxirribonuclemia.1,4
- En los receptores de TCMH alogénicos, la infección y la enfermedad por el CMV pueden llevar a diversas complicaciones y son causas importantes de morbilidad y mortalidad.1,5
- Se considera que hay una enfermedad por CMV cuando signos y síntomas clínicos están presentes y cuando se detecta el CMV en los tejidos del órgano respectivo en el receptor del trasplante.1,5
- La enfermedad de órgano terminal por CMV puede incluir neumonía, enfermedad gastrointestinal, encefalitis, hepatitis y retinitis por CMV.1
- La reactivación del CMV y la viremia por CMV de cualquier nivel se asocian con un mayor riesgo de mortalidad en los receptores de TCMH alogénicos durante el primer año posterior al trasplante.5
- Se ha demostrado reactivación del CMV poco después del trasplante; en más del 30% de los receptores de TCMH que eran seropositivos al CMV o tenían un donador seropositivo, se ha detectado infección por CMV menos de un mes después del trasplante.5
- En otro estudio, en el que se evaluó la incidencia de reactivación del CMV hasta 100 días después del trasplante, se descubrió que la reactivación se presentó desde el mismo día del trasplante (día 0).6
- En los receptores de trasplantes de células madre hematopoyéticas (TCMH) alogénicos, la seropositividad al CMV (R+) es un importante factor predictivo de infección primaria por CMV y reactivación del mismo.7,8
- Se ha demostrado que se presenta infección por CMV en aproximadamente 30% a 65% de los receptores de TCMH alogénicos seropositivos al virus que no reciben profilaxis.3,9
Proporción de infección por CMV en receptores
de TCMH alogénicos seropositivos al CMV3,9
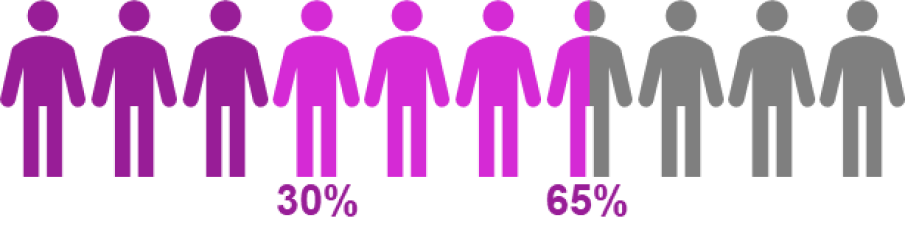
Estos hallazgos se apoyaron en dos estudios retrospectivos. El primero fue un análisis retrospectivo multivariable de datos de la base de datos del CIBMTR (Centro para la Investigación Internacional sobre la Sangre y el Trasplante de Médula Ósea, por sus siglas en inglés) sobre pacientes que recibieron su primer TCMH alogénico entre 2003 y 2010 (n=9,469), y el segundo fue un estudio retrospectivo de cohortes de 305 receptores de TCMH alogénicos entre enero de 2008 y diciembre de 2012.3,9
- En un estudio en el que se evaluó la incidencia de reactivación del CMV hasta 100 días después del trasplante, se encontró que la reactivación se presentó desde el mismo día del trasplante (día 0).1
La infección por CMV puede ocurrir tan temprano como el día 0 después del trasplante.1
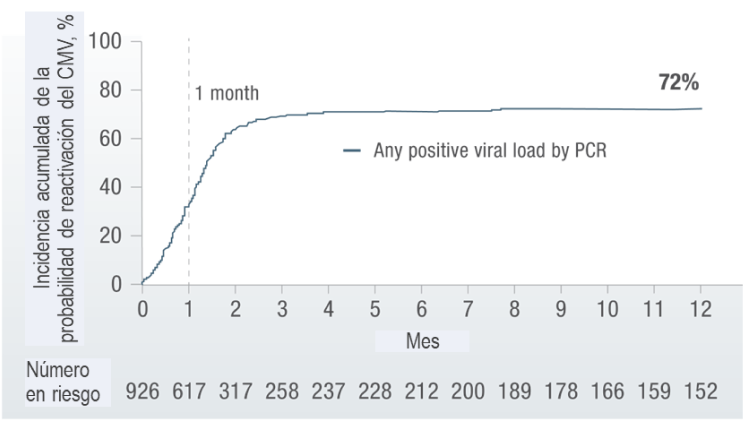
- En otro estudio retrospectivo se observó que más del 30% de los receptores de TCMH alogénicos que eran seropositivos al CMV o tenían un donador seropositivo experimentaron viremia por CMV menos de 1 mes después del trasplante.5
- Se presentó reactivación del CMV, definida por viremia de cualquier nivel, en 643 receptores (69%) en el curso de los 100 días post‐trasplante.5
Diseño del estudio
- Hammerstrom y cols. fue un estudio retrospectivo de cohortes realizado en 115 receptores adultos consecutivos sometidos a un TCMH alogénico haploidéntico entre marzo de 2009 y abril de 2014, en el cual se evaluó la incidencia de reactivación del virus en los 100 días siguientes al trasplante.6
- Green y cols. fue un estudio retrospectivo de cohortes no intervencional en el que se evaluó a 926 receptores de TCMH alogénicos entre el 1 de enero de 2007 y el 28 de febrero de 2013.5
- Se observó durante 1 año después del trasplante a los receptores de TCMH alogénicos que eran seropositivos al CMV o tenían un donador seropositivo, en busca de enfermedad o muerte por CMV, con pruebas semanales de CMV mediante reacción en cadena de la polimerasa hasta 100 días después del trasplante.5
- Se inició el tratamiento presintomático a partir de un umbral de carga viral de 125 UI/ml.5
- Cualquier viremia positiva ha sido asociada con un mayor riesgo de mortalidad total y no debida a la recaída al cabo de 1 año post‐trasplante.5
– El límite inferior de detección para el análisis del estudio era de 20 UI/ml; sin embargo, se empleó el umbral mínimo de 150 UI/ml, ya que este era el límite inferior de cuantificación de los ensayos disponibles comercialmente.
Carga viral de CMV como factor de riesgo de mortalidad total dependiente del tiempo a 1 año después del trasplante (N=926)a
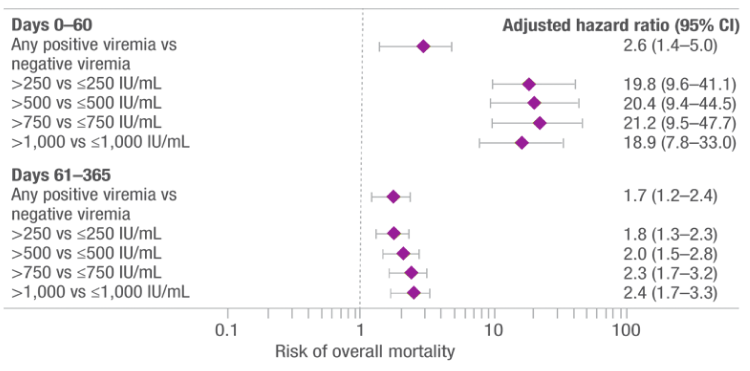
- Los resultados son de un estudio retrospectivo de cohortes no intervencional sobre mediciones de viremia por CMV y resultados clínicos recopilados anteriormente.
- Los receptores con cualquier nivel de viremia tuvieron un riesgo 2.6 veces mayor de mortalidad total que los receptores sin viremia.5
- A pesar del tratamiento presintomático, la mortalidad total acumulada a 1 año fue de 23.1% (IC de 95%, 20.1–26.1), según se observó en los 832 pacientes que sobrevivieron hasta el día 100.5
Diseño del estudio
- Este estudio retrospectivo de cohortes, unicéntrico y sin intervención abarcó a 926 receptores de TCMH alogénicos.5
- Se llevó a cabo un análisis retrospectivo multivariable de los datos de la base de datos del CIBMTR sobre trasplantes iniciales de células madre hematopoyéticas alogénicos realizados entre 2003 y 2010, para examinar las repercusiones de la seropositividad al CMV y su reactivación sobre la recaída de la enfermedad, la supervivencia total y la mortalidad no relacionada con la recaída.3
- La reactivación del CMV se asoció con una mortalidad más alta no debida a recaídas o mortalidad relacionada con el trasplante y una menor supervivencia total entre los grupos con todas las enfermedades: leucemia mielógena aguda y crónica (LMA, LMC), leucemia linfocítica aguda (LLA) y síndrome mielodisplásico (SMD).3
Reactivación del CMV como factor de riesgo de mortalidad no debida a recaídas y menor supervivencia total después de un TCMH alogénico (N=9,469)
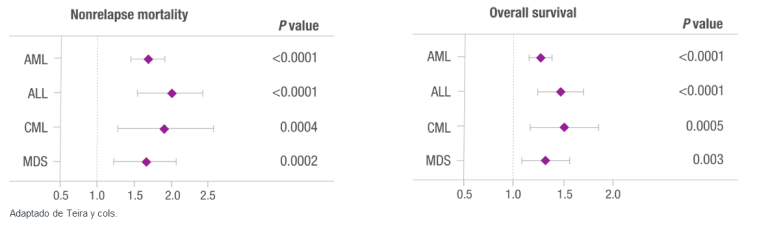
Limitaciones del estudio y hallazgos adicionales
- Limitaciones del estudio: no se recopiló información sobre cómo se vigiló la reactivación del CMV en relación con las pruebas empleadas y los valores aplicados para instituir el tratamiento; las prácticas institucionales para el tratamiento profiláctico y presintomático varían, lo que afecta la capacidad para evaluar la eficacia del tratamiento inicial y la duración de la reactivación del virus; la naturaleza retrospectiva del análisis limita la generalización de los resultados entre los distintos entornos de los trasplantes.
- En el estudio se observó que la reactivación del CMV no tuvo un efecto preventivo sobre la recaída del trastorno hematológico, independientemente del diagnóstico posterior al TCMH alogénico inicial.3
- En el contexto de la 7.a Conferencia Europea sobre Infecciones en la Leucemia (ECIL 7), se organizó un grupo de trabajo y se publicó la guía sobre diagnóstico, profilaxis y atención de la infección por CMV en los receptores de trasplantes de células madre hematopoyéticas (TCMH) y en los pacientes con neoplasias malignas hematológicas.10
- Debido al controvertido tema de que la infección por CMV se asocie con una reducción en la recaída leucémica después del TCMH, en las guías de la ECIL 7 se evaluó el papel del CMV en la recaída de la leucemia y no se descubrió efecto protector alguno del CMV respecto a dicha recaída.10
- En un amplio estudio multicéntrico retrospectivo en el que se evaluó la base de datos del CIBMTR, se encontró que la reactivación temprana del CMV no se asoció con recaída de la enfermedad entre los receptores de un TCMH alogénico en cuatro grupos de enfermedades: leucemia mielógena aguda, leucemia linfocítica aguda, leucemia mielógena crónica y síndrome mielodisplásico.3
- En las guías de la ECIL 7 se señala que no se recomiendan las estrategias permisivas de la reactivación del CMV para reducir las recaídas de la leucemia.10
Abreviaturas:
CIBMTR = Center for International Blood and Marrow Transplant Research (Centro para la Investigación Internacional sobre la
Sangre y el Trasplante de Médula Ósea, por sus siglas en inglés); ECIL 7 = 2017 European Conference on Infections in Leukaemia (Conferencia Europea sobre Infecciones en la Leucemia del 2017, por sus siglas en inglés); LLA = leucemia linfocítica aguda; LMA = leucemia mielógena aguda; LMC = leucemia mielógena crónica; PCR = reacción en cadena de la polimerasa; SMD = síndrome mielodisplásico; UI = unidades internacionales
Referencias:
- Ljungman P, Boeckh M, Hirsch HH y cols. Definitions of cytomegalovirus infection and disease in transplant patients for use in clinical trials. Clin Infect Dis. 2017;64(1):87–91.
- Crumpacker CS II. Cytomegalovirus (CMV). En: Bennet JE, Dolin R, Blaser MJ, eds. Mandell, Douglas, and Bennett’s Principles and Practice of Infectious Diseases. 8a. ed. Filadelfia, PA: Elsevier Inc; 2015:1738–1753.
- Teira P, Battiwalla M, Ramanathan M y cols. Early cytomegalovirus reactivation remains associated with increased transplant‐related mortality in the current era: a CIBMTR analysis. Blood. 2016;127(20):2427–2438.
- Ljungman P, Hakki M, Boeckh M. Cytomegalovirus in hematopoietic stem cell transplant recipients. Hematol Oncol Clin N Am. 2011;25:151–169.
- Green ML, Leisenring W, Xie H y cols. Cytomegalovirus viral load and mortality after haemopoietic stem cell transplantation in the era of pre‐emptive therapy: a retrospective cohort study. Lancet Haematol. 2016;3(3):e119–e127.
- Hammerstrom AE, Lombardi LR, Pingali SR y cols. Prevention of cytomegalovirus reactivation in haploidentical stem cell transplantation. Biol Blood Marrow Transplant. 2018;24(2):353–358.
- George B, Pati N, Gilroy N y cols. Pre‐transplant cytomegalovirus (CMV) serostatus remains the most important determinant of CMV reactivation after allogeneic hematopoietic stem cell transplantation in the era of surveillance and preemptive therapy. Transpl Infect Dis. 2010;12(4):322–329.
- Hakki M, Aitken SL, Danziger‐Isakov L y cols. American Society for Transplantation and Cellular Therapy Series: #3‐prevention of cytomegalovirus infection and disease after hematopoietic cell transplantation. Transplant Cell Ther. 2021:27:707‐719. doi: 10.1016/j.jtct.2021.05.001
- Sousa H, Boutolleau D, Ribeiro J y cols. Cytomegalovirus infection in patients who underwent allogeneic hematopoietic stem cell transplantation in Portugal: a five‐year retrospective review. Biol Blood Marrow Transplant.2014;20(12):1958–1967.
- Ljungman P, de la Camara R, Robin C y cols. Guidelines for the management of cytomegalovirus infection in patients with haematological malignancies and after stem cell transplantation from the 2017 European Conference on Infections in Leukaemia (ECIL 7). Lancet Infect Dis. 2019. doi:10.1016/S1473‐3099(19)30107‐0.